您现在的位置是: 首页 > 教育改革 教育改革
高考石油考点,考石油大学高中选文理
tamoadmin 2024-06-02 人已围观
简介1.关于石油价格上涨的影响(高考政治题)2.高考地理高频考点总结3.2023年大庆高考考点是哪里4.北京高考考点5.高考化学考点归纳分析?6.廊坊成人高考考点在哪考点一般设在设区市和华北石油管理局、定州市、辛集市政府所在地。因今年疫情防控要求,部分学校实行封闭管理,不能设为考点。由于报考人数较多,在主城区考点容纳不下的情况下,为保障考试顺利进行,部分市按照教育部有关规定,在县(市)政府所在地设立了
1.关于石油价格上涨的影响(高考政治题)
2.高考地理高频考点总结
3.2023年大庆高考考点是哪里
4.北京高考考点
5.高考化学考点归纳分析?
6.廊坊成人高考考点在哪
考点一般设在设区市和华北石油管理局、定州市、辛集市政府所在地。
因今年疫情防控要求,部分学校实行封闭管理,不能设为考点。由于报考人数较多,在主城区考点容纳不下的情况下,为保障考试顺利进行,部分市按照教育部有关规定,在县(市)政府所在地设立了考点。具体考点安排由市级招生考试机构统筹确定。
提醒考生要在规定时间内及时打印《准考证》,了解考点考场安排,提前一天到达考点所在地,熟悉考点环境、安排好食宿,以免因雨雾天气、道路交通维修或其他不可预测的原因影响正常考试。
考试期间,允许考生佩戴口罩参加考试,但在监考人员进行身份核查时须取下口罩主动配合检查。如在参加考试过程中出现发热、咳嗽等呼吸道症状者,应及时向监考人员报告。经现场医疗卫生专业人员评估后,综合研判是否具备参加考试条件,并按疫情防控工作要求进行处置。
关于石油价格上涨的影响(高考政治题)
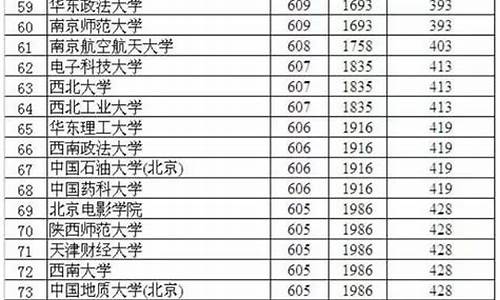
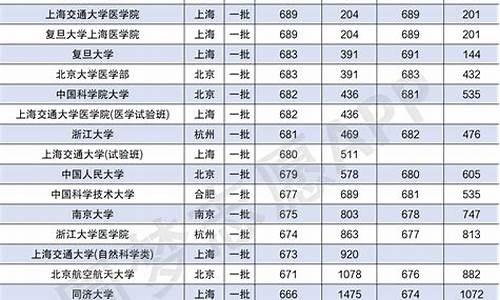
08年的数据要等到08年高考报名以后才知道,目前是无法知道的,天津07年普通高考全市报名总数为88500余人,比06年增加5000余人,这是在连续多年增幅在两位数基础上的首次降低。其中,文史类报考24800余人,比06年增加30余人,增幅约为0.1%;理工类报考59700余人,比06年增加4600余人,增幅约为8%;艺术体育类报考人数比06年增加100余人。
而天津07年高考
区县 考点名称 考点地点和电话
和平 二南开 和平区荣安大街167号 27314271
和平 二十一中学 和平区西宁道10号 27817007
和平 汇文中学 和平区甘肃路42号 27319815
和平 星座中学 和平区气象台路同安道13号 23532643
和平 耀华中学 和平区南京路89号 23396852
和平 一中 和平区西安道117号 23391126
河东 八十二中学 河东区大桥道八纬北路3号 24128181
河东 津华中学 河东区向阳楼晨阳道 24342966
河东 七中 河东区成林道30号 24316335
河东 四十五中学 河东区广宁路15号 84233061
河东 五十四中学 河东区六纬路135号 24313214
河西 北师大天津附中 河西区大沽南路1010号 13602018666
河西 实验中学 河西区平山道1号 23358689
河西 四十二中学 河西区大沽南路837号 13602116492
河西 四十一中学 河西区马场道195号 23280406
河西 四中 河西区隆昌路3号 28221910
河西 新华中学 河西区马场道99号 23288278
南开 第九中学复康路校区 南开区复康路5号 23522349
南开 二十五中学灵隐道校区 南开区灵隐道14号 27459907
南开 南开中学 南开区南开四马路22号 27483391
南开 七十四中学 南开区黄河道452号 13323325528
南开 三十一中学鼓楼西侧校区 南开区鼓楼西侧城北路 27333149
南开 四十三中学 南开区三潭路165号 60264351
南开 天津中学 南开区华苑中孚路41号 23728030
南开 一零九中学南丰路校区 南开区鞍山西道南丰路178号 27457330
河北 二中 河北区昆纬路141号 26235230
河北 扶轮中学 河北区吕纬路93号 26355033
河北 红光中学 河北区建昌道24号 26784040
河北 七十八中学 河北区增产道23号 26432240
河北 求真中学 河北区真理道六号路7号 26441637
河北 双建中学 河北区宙纬路46号 26236258
河北 天慈中学 河北区昆纬路46号 26235866
河北 五十七中学 河北区昆纬路38号 26236304
河北 五十七中学月纬路校区 河北区月纬路46号 26236328
红桥 八十中学北院 红桥区光荣道39号 26371337
红桥 复兴中学 红桥区隆春里春和路1号 87726071
红桥 民族中学 红桥区西青道87号 27733938
红桥 三中 红桥区一号路向东道1号 26370695
红桥 五十一中学南院 红桥区芥园道习艺所南街4号 27710521
红桥 五中 红桥区北大街58号 86513076
塘沽 塘沽二中 塘沽区浙江路74号 25861758
塘沽 塘沽十三中 塘沽区广州道开源里21号 66308422
塘沽 塘沽一中 塘沽区烟台道3号 25863962
汉沽 汉沽八中 汉沽区文化街 67194197
汉沽 汉沽一中 汉沽区文化街 67194200
大港 大港实验中学 大港区世纪大道191号 63386641
大港 大港一中 大港区世纪大道东 63239009
大港 华油一中 华北石油会战道 0317-2724467
东丽 一百中学 东丽区津塘二线开发区 84933855
西青 二中 西青区杨柳青柳口路与一中路交口 27391603
西青 杨柳青三中 西青区杨柳青新华道175号 27391606
西青 杨柳青一中 西青区杨柳青汇文路1号 27391600
津南 咸水沽一中 津南区咸水沽镇津岐路全红桥旁 28395048
北辰 华辰学校 北辰区京津公路517号 26834747
北辰 四十七中学 北辰区京津公路富锦道南口 26918821
宁河 芦台二中 宁河县芦台镇振新路30号 69564329
宁河 芦台一中 宁河县芦台镇一中路 69591013
武清 杨村六中 武清区杨村镇 82162517
武清 杨村七中 武清区杨村镇 82191667
武清 杨村三中 武清区杨村镇 29342310
武清 杨村五中 武清区杨村镇 59616713
武清 杨村一中 武清区杨村镇 59611155
静海 静海二中 静海镇胜利北路5号 28942603
静海 静海四中 静海镇胜利大街南 28944988
静海 静海一中 静海镇地纬路东段 68600513
静海 模范学校 静海镇地纬路东段 68603084
宝坻 宝坻三中 宝坻区建设路西段 29262362
宝坻 宝坻四中 宝坻区进京路30号 82621377
宝坻 宝坻一中 宝坻区海滨街道北城东路 29228600
宝坻 宝坻育英中学 宝坻区南关大街20号 29241679
宝坻 宝坻中专 宝坻区进京路28号 82621469
蓟县 蓟县城关二中 蓟县城内人民东路 82822711
蓟县 蓟县城关四中 蓟县城内兴华大街 82862252
蓟县 蓟县实验中学 蓟县城内花园里二段 29031376
蓟县 蓟县燕山中学 蓟县城西 29030633
蓟县 蓟县一中 蓟县城内迎宾路 29146214
蓟县 蓟县渔阳中学 蓟县城内迎宾路 29142320
蓟县 蓟县中专 蓟县城西 29172955
蓟县 蓟州中学 蓟县渔阳南路 29032513
海滨中心 油田一中 大港油田二号院 25921169
天津铁厂 铁厂二中 河北省涉县天津铁厂 0310-3973127
高考地理高频考点总结
受到投资者担心原油供应紧张以及美元贬值等因素影响,国际原油期货价格2日在历史上首度突破每桶100美元大关。一段时间以来,高油价飓风一直冲击着中国,投资者关心的是:中国经济能够承受100美元的油价之重?早在去年11月1日,发改委就曾将汽油、柴油 和航空煤油价格每吨各提高500元以应对国际油价冲击。具体到行业个股影响而言,孕育着哪些风险与机遇?
国际原油期价首次突破100美元大关
国际油价在2008年第一个交易日大幅上涨。到美国东部时间2日中午12点06分左右,纽约商品交易所2月份交货的轻质原油期货价格在电子交易中达到每桶100美元,这一价格刷新了2007年创出的每桶99.29美元的国际原油期货盘中最高记录。
多种因素导致国际原油价格大涨。非洲主要产油国尼日利亚国内局势持续动荡,武装分子1日袭击了该国主要产油区,导致多人死亡。石油输出国组织(欧佩克)2日警告说,到2024年,该组织可能无法满足国际原油市场需求。此外,美元对西方主要国家货币当天继续贬值,国际黄金以及主要商品期货价格继续走高。(新华网)
油价上涨直接影响的行业
油价直接或者间接影响的行业范围较大,在油价上涨的大背景下,油价上调的相关受益板块必然会在二级市场上有相应表现。而投资者重视油价受益板块,则可以在08年行情中获得较好的结构性获利机会。
1,直接受益行业
石油开采业、石油设备制造和石油运输行业,无疑是油价上涨的直接受益者。首先,作为上游行业的石油开采行业,无疑是最直接受益于油价上涨。其次,石油价格高涨也直接促进石油开发的加快,因此石油开采相关的设备制造及石油运输行业,都必然受益于行业景气度的提高。这一板块具体包括原油开采企业、石油工程承包商、石油机械制造商、油田修理和管道输送等企业。而目前两市中这类上市公司并不多,屈指可数的几家值得关注。
2,能源替代行业
煤炭无疑在相关能源产品中具有最大替代作用,而由于资源总体需求增加和具备相似性特征产品(石油)的价格提高,促使煤炭价格不断走高。而电力及其它替代类能源行业,无疑也是在油价上涨过程中的主要间接受益板块。尤其是不受到煤炭、石油价格上调影响的水电类上市公司、新能源等行业。
3,能够消化油价上涨压力的上市公司
如航空业等,表面在油价上涨过程中,由于占其成本比例较大的航油价格上涨可能受到损害,但实际情况并非如此。一方面,国内航油价格处于管制状态,航油价格未必会随着油价同比上调,加上燃油附加费,实际上是帮助航空公司完全消化了成本提高的压力。另外一方面在经济发展偏热、油价上涨的背景下,航空公司的客座率提高和票价折扣降低(也就是实际上的涨价),反而搞高了航空公司的利润水平。
另外,高油价对煤化工、电石化工行业也形成实质性利好。在油价上涨的过程中,以煤炭为原材料的煤化工企业相对于以石油天然气为原料的化工企业,其成本成本优势明显凸现出来。包括煤焦油、合成氨、甲醇等,而其产品随着油价的提升反而可获得相应的提价空间。尤其是生产PVC、PTA、MDI等存在供给缺口的公司,调价能力强,更是值得关注。(广州万隆)
2023年大庆高考考点是哪里
对于高考地理的提分方法来说,最有效的方法就是能够掌握一些高频的地理知识点了,下面我为大家整理了一些高考地理必备的知识考点。
高考地理地图方面重要知识点总结
地图专题1.经度的递变:向东度数增大为东经度,向西度数增大为西经度。
2.纬度的递变:向北度数增大为北纬度,向南度数增大为南纬度。
3.纬线的形状和长度:互相平行的圆,赤道是最长的纬线圈,由此往两极逐渐缩短。
4.经线的形状和长度:所有经线都是交於南北极点的半圆,长度都相等。
5.东西经的判断:沿著自转方向增大的是东经,减小的是西经。
6.南北纬的判断:度数向北增大为北纬,向南增大为南纬。
7.东西半球的划分:20°W往东至160°E为东半球,20°W往西至160°E为西半球。
8.东西方向的判断:劣弧定律(例如东经80°在东经1°的东面,在西经170°的西面)
9.比例尺大小与图示范围:相同图幅,比例尺愈大,表示的范围愈小;比例尺愈小,表示的范围愈大。
10.地图上方向的确定:一般情况,“上北下南,左西右东”;有指向标的地图,指向标的箭头指向北方;经纬网地图,经线指示南北方向,纬线指示东西方向。
11.等值线的疏密:同一幅图中等高线越密,坡度越陡;等压线越密,风力越大;等温线越密,温差越大
12.等高线的凸向与地形:等高线向高处凸出的地方为山谷,向低处凸出的地方为山脊。
13.等高线的凸向与河流:等高线凸出方向与河流流向相反。
14.等温线的凸向与洋流:等温线凸出方向与洋流流向相同。
高考地理如何学习?史上最强高考励志书《高考蝶变》教你怎样提高成绩,淘宝搜索《高考蝶变》购买。
高考地理必备五大知识点高考必背地理大题:分析朝鲜半岛南北在地形、气候、植被、经济等方面的异同点?
地形:以山地为主,地势东北高、西南低。气候:南部——亚热带季风气候;北部——温带季风气候。植被:南部——亚热带常绿阔叶林;北部——温带落叶阔叶林。经济:南部发达的资本主义国家,北部经济相对落后的社会主义国家。
高考地理日本工业分布在哪里?原因?
濑户内海和太平洋沿岸。原因:①日本国土小,矿产资源缺乏,需进口;②日本为岛国,海岸线曲折,濑户内海和太平洋沿岸多优良港口;③日本市场小,需出口工业品。19.东南亚的经纬度范围?(90°E~140°E,25°N~10°S)
东亚沿海地区农业发达的原因?(提示:从地形、气候、土壤、人口、历史方面分析)
地形;平原为主,地势平坦。便于耕种。气候:季风气候,雨热同期,适于农作物生长。土壤:肥沃。人口:众多,劳动力丰富。历史:农业发展历史悠久。
对我国石油运输而言,中缅输油管道、克拉地峡运河航线与马六甲海峡航线相比有哪些优势?
我国石油主要是从中东地区进口,即石油进口线路主要是马六甲海峡航线。中缅输油管道线路、克拉地峡运河航线比马六甲海峡航线距离短,可节省运输时间和能源;且中缅输油管道线路一部分在中国和缅甸境内,在陆地上进行管道运输,可摆脱过份依靠马六甲海峡航线的局面。
泛亚铁路的起始点、所穿过地区地质方面的不利条件,以及修建的意义?
困难:①地形崎岖;②火山地震多;③滑坡泥石流多。意义:①加强了各国间的贸易往来和经济发展;②使我国云南和东盟各国拥有陆上贸易通道,缩短了内陆省份南下印度洋的运输距离,有利于扩大我国的对外开放。
北京高考考点
2023年大庆高考考点可在教育网进行查询。
2023年高考的考点如下:
1、语文通常包括阅读理解、作文和文学常识等多个板块,需要考生具备较为全面的语文素养。考点有:阅读理解:一定要理解文章的中心思想,掌握文章的结构和要点。
作文:要注意提高写作水平,增加修辞手法和语言表达能力。文学常识:作为语文的重要组成部分,考生需要熟练掌握中国古代文学、现代文学和外国文学的基本概念和知识。
2、数学考试通常包括数与式、函数与方程、几何、概率与统计四个板块,要求考生掌握数学的基本概念和运算能力。考点有:数学基本概念:不同板块的内容 具有一定的联系,各方面都要融汇贯通。
基本运算:要熟练掌握常用的运算方法,有意识地开展复习练习知识点的拓展能力。应用题:要具备解题的能力,对各种样式的应用型题目具有丰富的经验积累。
3、英语考试通常包括听、说、读、写四个板块,需要考生掌握英语的基本语法和词汇,同时还需要具备一定的交际能力。考点有:语音语调:要注意语言的音准和语调、发音和语音。
词汇和语法:需要掌握足够的基础词汇和语法知识,以便理解大量的文本阅读材料。综合能力:需要考生具备一定的综合能力,能够在听、说、读、写四个方面全面掌握英语的基础知识,提高英语应用能力。
高考需要注意以下几点事项:
1、正确理解高考改革。要密切跟踪高考政策变化,理解高考考试方式与考点设置的新变化。特别要注意选修课和热点领域知识的考查要求。这有助于制定更加科学的复习计划。
2、选择适合的高考备考资料。要选择权威和适合考生水平的高考备考教材与资料。要根据高考考点设置选择重点复习的内容与课题。
3、制定科学的复习计划。要制定具体可行的日复习计划和总复习计划。重点安排考点与薄点的复习进度,确保知识面覆盖到位。计划要有针对性且兼顾天数充裕度。
4、采用科学的复习方法。要结合高考考试形式,采用题海练习、模拟练习等方法。只有大量实战练习,才能熟练掌握知识与技巧。
5、管理好心态。高考临近要注意调整好心态,保持积极乐观与镇定状态。避免过于焦虑与紧张,要相信自己已付出的努力并努力发挥正常水平。
6、严格考前准备。考试前一天要规范作息,早睡早起。带好所需文具,考前要再次确认考场位置与交通时间。做好最终的心理建设,在进入考场时做到心态平和。
高考化学考点归纳分析?
关于北京高考考点,相关内容如下:
北京高考考点包括:北京市各区县的教育考试院、各高校(如清华大学、北京大学等)、北京体育大学、对外经济贸易大学、中国人民大学、北京师范大学等。
1.北京市各区县的考点
北京市各区县的教育考试院均设有高考考点,共计36个。每个考点都有具体地址和交通路线,考生可以根据自己所在地理位置和交通条件选择就近的考点。
2.各高校作为考点
清华大学、北京大学等高校均作为高考考点,这些高校作为优质的考点也能够提高考生参加高考的心理素质,对于他们未来的学习和发展也将会起到积极的影响。
3.北京体育大学和对外经济贸易大学
北京体育大学和对外经济贸易大学也作为高考考点存在。对于有志于体育、经济或者其他相关专业的考生而言,选择这些考点进行高考将更有利于他们未来的学习和发展。
4.中国人民大学和北京师范大学
中国人民大学和北京师范大学虽然不是北京高考的主要考点,但也有部分考生在这些学校进行高考。对于有志于文科或者社会科学等相关专业的考生而言,选择在这些学校进行高考将更有利于他们未来的学习和发展。
6.如何选择合适的考点
对于考生而言,如何选择一个合适的高考考点非常重要。首先,考生应该根据自己所在地理位置和交通条件选择就近的考点,以便降低旅途中的压力和疲劳。
其次,考生应该了解各个考点的环境和设施,如是否有自习室、休息室、饮水设备等,这些设施能够为考生提供方便和舒适的学习环境。此外,还应该考虑考点的安全性和监考质量,以保障自己的考试成绩不受到任何影响。
7.高考考场禁物清单
高考是一项严肃的考试,考场上有很多的禁止事项,如果考生在考试过程中违反了禁止事项,将会得到警告或者取消该科目的考试资格。在高考中,考生应该遵守以下禁物清单:
禁止携带手机、电子设备、无线通讯设备等通讯工具;禁止携带纸张、书籍、参考资料等与考试无关物品;禁止携带食品、饮料等物品;禁止在考场上交头接耳、传纸条等行为;禁止带走任何考试材料和试卷;禁止在考场上行走和扰动考生。
总之,考生应该严格遵守高考考场规定,保证自己的考试公正、安全和顺利进行。
总结:
北京高考考点包括了北京市各区县的教育考试院、各高校以及其他一些知名大学和高等学府。选择合适的考点不仅能够帮助考生更好地完成高考,同时也能够提升其心理素质和未来的学习和发展。
廊坊成人高考考点在哪
考点是我们复习化学的过程中最近注意的重要知识点。下面是我为您带来的,希望对大家有所帮助。
:
1:各种“水”汇集
一纯净物:
重水D2O;超重水T2O;蒸馏水H2O;双氧水H2O2;水银Hg;水晶SiO2。
二混合物:
氨水分子:NH3、H2O、NH3·H2O;离子:NH4 、OH?、H
氯水分子:Cl2、H2O、HClO;离子:H 、Cl?、ClO?、OH?
王水浓HNO3∶浓HCl=1∶3溶质的体积比 卤水MgCl2、NaCl及少量MgSO4
硬水溶有较多量Ca2 、Mg2 的水 软水溶有较少量或不溶有Ca2 、Mg2 的水
铁水Fe、C、Mn、Si、S、P等单质的熔融态混合体
苏打水Na2CO3的溶液 生理盐水0.9%的NaCl溶液 硝盐镪水[浓硝盐酸]
水玻璃Na2SiO3水溶液 水泥2CaO·SiO2、3CaO·SiO2、3CaO·Al2O3
2:各种“气”汇集
一 无机的:爆鸣气H2与O2;水煤气或煤气CO与H2;高炉气或高炉煤气CO、CO2、N2
笑气N2O 碳酸气CO2
二有机的:天然气又叫沼气、坑气,主要成分为CH4 电石气CH≡CH,常含有H2S、PH3等
裂化气C1~C4的烷烃、烯烃 裂解气CH2=CH2、CH3CH=CH2、CH2=CHCH=CH2等
焦炉气H2、CH4等 炼厂气C1~C4的气态烃,又叫石油气、油田气。
3:氧化物的分类
一氧化物的分类:成盐氧化物:酸性氧化物、碱性氧化物、两性氧化物、复杂氧化物过氧化物、超氧化物、Fe3O4、Pb3O4等;不成盐氧化物CO、NO
二易混淆概念分辨
酸酐不一定是酸性氧化物:如乙酸酐酐CH3CO2O等;酸性氧化物一定是酸酐。
非金属氧化物不一定是酸性氧化物:如NO、CO、NO2、N2O4、H2O
酸性氧化物不一定是非金属氧化物:如Mn2O7、CrO3
金属氧化物不一定是碱性氧化物:如Al2O3、ZnO两性,Mn2O7、CrO3酸性氧化物
碱性氧化物一定是金属氧化物
※NO2因与碱反应不仅生成盐和水,还有NO,因而不是酸性氧化物。
※Na2O2因与酸反应不仅生成盐和水,还有O2,因而不是碱性氧化物。
4:比较金属性强弱的依据
1、同周期中,从左到右,随核电荷数的增加,非金属性增强; 同主族中,由上到下,随核电荷数的增加,非金属性减弱;
2、依据最高价氧化物的水化物酸性的强弱:酸性愈强,其元素的非金属性也愈强;
3、依据其气态氢化物的稳定性:稳定性愈强,非金属性愈强;
4、与氢气化合的条件;5、与盐溶液之间的置换反应;
6、其他,例:2Cu+S , Cu+Cl2 所以,Cl的非金属性强于S。
6:“10电子”、“18电子”的微粒小结
分子 离子
一核10电子的 Ne N3?、O2?、F?、Na 、Mg2 、Al3
二核10电子的 HF OH- 三核10电子的 H2O NH2-
四核10电子的 NH3 H3O 五核10电子的 CH4 NH4
分子 离子
一核18电子的 Ar K 、Ca2 、Cl?、S2?
二核18电子的 HCl HS- 三核18电子的 H2S、F2
四核18电子的 PH3 五核18电子的 SiH4 、CH3F PH4
六核18电子的 N2H4、CH3OH 注:其它诸如C2H6、N2H5 、N2H62 等亦为18电子的微粒。
7:具有漂白作用的物质
氧化作用:Cl2、O3、Na2O2、浓HNO3;化学变化;不可逆
化合作用:SO2;化学变化;可逆 吸附作用:活性炭;物理变化;可逆
其中能氧化指示剂而使指示剂褪色的主要有Cl2HClO和浓HNO3及Na2O2
8:安全火柴的成分及优点
安全火柴的成分:火柴头:氧化剂K、MnO2、易燃物如硫等、粘合剂
火柴盒侧面:红磷、三硫化二锑、粘合剂 起火原因:摩擦→发热→KClO3分解→使红磷着火→引起火柴头上的易燃物如硫燃烧。 优点:红磷与氧化剂分开,比较安全,无毒性。
9:能升华的物质
I2、干冰固态CO2、升华硫、红磷,萘。蒽和苯甲酸作一般了解。
10:能被活性炭吸附的物质
1、有毒气体NO2、Cl2、NO等——去毒;
2、 色素——漂白; 3、水中有臭味的物质——净化。
11:矽及其化合物十“反常”
1、矽的还原性比碳强,而碳在高温下却能从二氧化矽中还原出矽。SiO2+2C=Si+2CO↑
2、非金属单质一般不与弱氧化性酸反应,而矽不但能与HF反应,而且还有H2生成。Si+4HF=SiF4↑+2H2↑
3、非金属单质与强碱溶液反应一般不生成氢气,而矽却不然。Si+2NaOH+H2O==Na2SiO3+2 H2↑
4、虽然SiO2是矽酸的酸酐,但却不能用SiO2与水反应制备矽酸,只能用可溶性矽酸盐跟酸作用来制备。
5、酸性氧化物一般不与酸反应除氧化还原反应外,而二氧化矽却能与氢氟酸反应。
6、非金属氧化物一般是分子晶体,而二氧化矽却是原子晶体。
7、无机酸一般易溶于水,而矽酸和原矽酸却难溶于水。
8、通常所说的某酸盐为一种酸根的盐,而矽酸盐却是多种矽酸H2SiO3、H4SiO4、H2Si2O5、H6Si2O7等的盐的总称。
9、较强的酸能把较弱的酸从其盐溶液中制取出来,这是复分解反应的一般规律,由此对于反应Na2SiO3+CO2+H2O==Na2CO3+H4SiO4↓的发生是不难理解的,而反应Na2CO3+SiO2=Na2SiO3+CO2↑居然也能进行。
10、矽酸钠的水溶液俗称水玻璃,但它和玻璃的化学成分并不相同。矽酸钠也叫泡花碱,但它是盐而不是碱。钢化玻璃与普通玻璃成分相同,水晶玻璃与玻璃成分不同。
12:碱金属元素具体知识的一般与特殊
1、Na、K均储存在煤油中,防止氧化,但锂单质不能储存在煤油中,因锂单质密度小于煤油,浮于煤油液面,达不到隔绝空气的目的,应储存太平石蜡中。
2、碱金属单质的密度一般随核电荷数的增大而增大,但钾的密度却比钠小。
3、碱金属单质在空气中燃烧大部分生成过氧化物或超氧化物,但锂单质特殊,燃烧后的产物只是普通氧化物。
4、碱金属单质和水反应时,碱金属一般熔点较低,会熔化成小球。但锂的熔点高,不会熔成小球。生成的LiOH溶解度较小,覆盖在锂的表面,使锂和水的反应不易连续进行。
5、碱金属单质和水反应时,碱金属单质一般浮于水面上,但铷、铯等单质和水反应时沉入水底,因铷、铯单质的密度比水大。
6、钠盐的溶解度受温度的变化影响一般都较大,但NaCl的溶解度受温度变化的影响却很小。
7、碱金属的盐一般均易溶于水,但Li2CO3却微溶于水。
8、焰色反应称为“反应”,但却是元素的一种物理性质。
13:Fe3 的颜色变化
1、向FeCl3溶液中加几滴KSCN溶液呈红色;2、FeCl3溶液与NaOH溶液反应,生成红褐色沉淀;
3、向FeCl3溶液溶液中通入H2S气体,生成淡**沉淀;
4、向FeCl3溶液中加入几滴Na2S溶液,生成淡**沉淀;当加入的Na2S溶液过量时,又生成黑色沉淀;
5、向FeCl3溶液中加入过量Fe粉时,溶液变浅绿色;
6、向FeCl3溶液中加入过量Cu粉,溶液变蓝绿色; 7、将FeCl3溶液滴入淀粉KI溶液中,溶液变蓝色;
8、向FeCl3溶液中滴入苯酚溶液,溶液变紫色;
14:“黑色金属”有哪些
化学上把铁、铬、锰三种金属和铁基合金统称为“黑色金属”。
15:Fe2 与Fe3 的鉴别方法
Fe2 与Fe3 的性质不同而又可以相互转化。中学化学中可用以下几种方法加以鉴别。
1.观察法:其溶液呈棕**者是Fe3 ,呈浅绿色者是Fe2 。
2.H2S法:通往H2S气体或加入氢硫酸,有浅**沉淀析出者是Fe3 ,而Fe2 溶液 不反应。2Fe3 +H2S==2Fe2+2H +S↓
3.KSCN法:加入KSCN或其它可溶性硫氰化物溶液,呈血红色者是Fe3 溶液,而Fe2 的溶液无此现象。这是鉴别鉴别Fe3 与Fe2 最常用、最灵敏的方法。Fe3 +SCN?==[FeSCN]2
4.苯酚法:分别加入苯酚溶液,显透明紫色的是Fe3 溶液,无此现象的是Fe2 的溶液。Fe3+6C6H5OH→[FeC6H5O6]3?+6H 了解
5.碱液法:取两种溶液分别通入氨气或碱液,生成红褐色沉淀的是Fe3 溶液,生成白色沉淀并迅速变为灰绿色、最终变成红褐色的是Fe2 溶液。 Fe3 +3NH3·H2O==FeOH3↓+3NH4 ;
Fe3 +3OH?== FeOH3↓ Fe2 +2 NH3·H2O==FeOH2↓+2NH4 ;4 FeOH2+2H2O+O2==4 FeOH3
6.淀粉KI试纸法:能使淀粉KI试纸变蓝的是Fe3 溶液,无变化的是Fe3 溶液。2 Fe3 +2I?==2 Fe2 +I2
7.铜片法:分别加入铜片,铜片溶解且溶液渐渐变为蓝色的是Fe3 溶液,无明显现象的是Fe2 溶液。
2 Fe3 +Cu==2 Fe2 +Cu2
8.KMnO4法:分别加入少量酸性KMnO4溶液,振荡,能使KMnO4溶液紫红色变浅的是Fe2 溶液,颜色不变浅的是Fe3 溶液。5 Fe2 +MnO4?+8H ==5 Fe3 +Mn2 +4H2O
16:金属的冶炼规律
1.活泼金属的冶炼 钠、镁、铝等活泼金属,采用电解其熔融态的卤化物的方法冶炼通直流电。
例如:2NaCl熔融 2Na+Cl2↑ MgCl2熔融 Mg+Cl2↑
2Al2O3熔融 4Al+3O2↑加入Na3AlF6作熔剂
注:这里为何不电解熔融态铝的氯化物而须电解其熔融态的氧化物,读者应掌握AlCl3为共价化合物,熔融态时不电离,而Al2O3为离子化合物,熔融态时可发生电离的道理。
2.中等活泼的金属的冶炼 锌、铁、锡、铅等中等活泼的金属采用还原剂还原它们的氧化物的方法冶炼。
例如:ZnO+C Zn+CO↑ Fe2O3+3CO 2Fe+3CO2 WO3+3H2 W+3H2O
Cr2O3+2Al 2Cr+Al2O3
3.不活泼金属的冶炼 银、铂、金等不活泼金属在自然界可以游离态存在,直接采用物理方法如淘金等冶炼,而铜、汞等不活泼金属可用还原剂还原法或热分解法冶炼。例如:2HgO 2Hg+O2↑
17:“置换反应”有哪些?
1.较活泼金属单质与不活泼金属阳离子间置换 如:Zn+Cu2 ==Zn2 +Cu Cu+2Ag =2Ag
2、活泼非金属单质与不活泼非金属阴离子间置换Cl2 2Br?==2Cl? Br2
I2 S2?==2I? S 2F2+2H2O==4HF+O2
3、 活泼金属与弱氧化性酸中H 置换 2Al+6H ==2Al3?+3H2↑
Zn+2CH3COOH==Zn2 +2CH3COO?+H2↑
4、金属单质与其它化合物间置换 2Mg+CO2 2MgO+C
2Mg+SO2 2MgO+S Mn+FeO MnO+Fe 2Na+2H2O==2Na +2OH?+H2↑
2Na+2C6H5OH熔融→2C6H5ONa+H2↑ 2Na+2C2H5OH→2C2H5ONa+H2↑
10Al+3V2O5 5Al2O3+6V 8Al+3Fe3O4 4Al2O3+9Fe
2FeBr2+3Cl2==2FeCl3+2Br2 2FeI2+ 3Br2==2FeBr3+2I2 Mg+2H2O MgOH2+H2↑
3Fe+4H2O气 Fe3O4+4 H2↑
5、 非金属单质与其它化合物间置换 H2S+X2==S↓+2H +2X?
2H2S+O2 2S+2H2OO2不足 CuO+ C Cu+CO↑ C过量时
2 CuO+C 2Cu+CO2↑ CuO过量时 FeO+ C Fe+CO↑
2FeO+Si SiO2+2Fe↑ 2FeO+C 2Fe+CO2↑ CuO+H2 Cu+H2O
Cu2O+H2 2Cu+H2O SiO2+2C Si+2CO↑ 3Cl2+8NH3==6NH4Cl+N2
3Cl2+2NH3==6HCl+N2
18:条件不同,生成物则不同
1、2P+3Cl2 2PCl3Cl2不足 ;2P+5Cl2 2PCl5Cl2充足
2、2H2S+3O2 2H2O+2SO2O2充足 ;2H2S+O2 2H2O+2SO2不充足
3、4Na+O2 2Na2O 2Na+O2 Na2O2
4、CaOH2+CO2 适量== CaCO3↓+H2O ;CaOH2+2CO2过量==CaHCO32↓
5、2Cl2+2 CaOH2==CaClO2+CaCl2+2H2O 6Cl2+6 CaOH2 CaClO32+5CaCl2+6H2O
6、C+O2 CO2O2充足 ;2C+O2 2CO O2不充足
7、8HNO3稀+3Cu==2NO↑+2CuNO32+4H2O 4HNO3浓+ Cu==2NO2↑+CuNO32+2H2O
8、NaCl固+H2SO4 浓NaHSO4+HCl↑ 2NaCl固+H2SO4 浓Na2SO4+2HCl↑
9、 H3PO4+ NaOH==NaH2PO4+H2O;H3PO4+2NaOH==Na2HPO4+2H2O
H3PO4+3NaOH==Na3PO4+3H2O
10、AlCl3+3NaOH==AlOH3↓+3NaCl ; AlCl3+4NaOH过量==NaAlO2+2H2O
11、NaAlO2+4HCl过量==NaCl+2H2O+AlCl3;NaAlO2+HCl+H2O==NaCl+AlOH3↓
12、Fe+6HNO3热、浓==FeNO33+3NO2↑+3H2O;Fe+HNO3冷、浓→钝化
13、Fe+6HNO3热、浓 FeNO33+3NO2↑+3H2O;Fe+4HNO3热、浓 FeNO32+2NO2↑+2H2O
14、Fe+4HNO3稀=FeNO33+NO↑+2H2O;3Fe+8HNO3稀=3FeNO33+2NO↑+4H2O
15、C2H5OH CH2=CH2↑+H2O C2H5-OH+HO-C2H5 C2H5-O-C2H5+H2O
16.苯与氯气反应
17、C2H5Cl+NaOH C2H5OH+NaCl C2H5Cl+NaOH CH2=CH2↑+NaCl+H2O
18、6FeBr2+3Cl2不足==4FeBr3+2FeCl3 2FeBr2+3Cl2过量==2Br2+2FeCl3
19:滴加顺序不同,现象不同
1、AgNO3与NH3·H2O:AgNO3向NH3·H2O中滴加——开始无白色沉淀,后产生白色沉淀
NH3·H2O向AgNO3中滴加——开始有白色沉淀,后白色沉淀消失2、CaOH2与H3PO4多元弱酸与强碱反应均有此情况:
CaOH2向H3PO4中滴加——开始无白色沉淀,后产生白色沉淀
H3PO4向CaOH2中滴加——开始有白色沉淀,后白色沉淀消失
3、NaOH与AlCl3:NaOH向AlCl3中滴加——开始有白色沉淀,后白色沉淀消失
AlCl3向NaOH中滴加——开始无白色沉淀,后产生白色沉淀4、HCl与NaAlO2:HCl向NaAlO2中滴加——开始有白色沉淀,后白色沉淀消失
NaAlO2向HCl中滴加——开始无白色沉淀,后产生白色沉淀5、Na2CO3与盐酸:Na2CO3向盐酸中滴加——开始有气泡,后不产生气泡
盐酸向Na2CO3中滴加——开始无气泡,后产生气泡20:有关“燃烧”的总结
一“燃烧”的条件:
1.温度达到着火点;2.有助燃剂多指在反应中的氧化剂
二镁在哪些气体中能燃烧?
1.镁在空气氧气中燃烧:2Mg+O2 2MgO 现象:产生白烟,发出耀眼的强光。
2.镁在氯气中燃烧:Mg+Cl2 MgCl2 现象:产生白烟。
3.镁在氮气中燃烧:3Mg+N2 Mg3N2 现象:产生灰**烟。
4.镁在CO2气体中燃烧:2Mg+CO2 2MgO+C现象:产生白烟,瓶壁上有少许淡**物质。
三火焰颜色小结:
H2在空气中燃烧淡蓝色;CH4在空气中燃烧淡蓝色;C2H4在空气中燃烧火焰明亮,黑烟
C2H2在空气中燃烧浓烈的黑烟;H2S在空气中燃烧淡蓝色;C2H5OH在空气中燃烧淡蓝色
S在空气中燃烧淡蓝色;S在纯氧中燃烧蓝紫色;CO在空气中燃烧淡蓝色
H2在Cl2中燃烧苍白色
此外:含钠元素的物质焰色呈**;含钾元素的物质焰色呈紫色透过蓝色钴玻璃片
2023年河北廊坊成人高考考点分布在安次区、广阳区、开发区、三河市、三河(燕郊)等地区。
1、安次区:
廊坊市第一中学:廊坊市安次区永兴南路288号。
廊坊市第八高级中学:廊坊市安次区西昌路103号。
2、广阳区:
廊坊市第七中学:廊坊市广阳区建设北路171号;
中国石油天然气管道局中学:廊坊市广阳区建国道350号。
3、开发区:
廊坊经济技术开发区新世纪中学:廊坊经济技术开发区四海路165号。
4、三河市:
三河市第一中学:三河市泃阳西大街243号;
三河市第三中学:河北三河市李旗庄镇第三中学。
5、三河(燕郊):
三河市第二中学:河北省三河市燕郊镇京哈路南38号。
成人高考需要准备
1、身份证明:携带身份证原件及复印件。
2、学历证明:本人最高学历毕业证书原件及相应复印件,
3、复习资料:根据所报考专业的考试科目进行复习,可选择购买正规出版社出版的教材或考试大纲进行学习。携带,0.5mm黑色签字笔2支、2B铅笔、橡皮、准考证等。