您现在的位置是: 首页 > 教育比较 教育比较
2010北京高考化学试题_2007北京高考化学
tamoadmin 2024-05-20 人已围观
简介我的理解碳酸氢铵溶液基本上是接近中性或者更偏酸性一点虽然氢氧化亚铁的离子积较低但是碳酸根的浓度更大所以会生成碳酸亚铁的沉淀还有一个问题氢氧化亚铁的溶度积=c(Fe2+)c(OH-)c(OH-)碳酸亚铁的溶度积=c(Fe2+)c(CO32-)无法得出氢氧化亚铁更容易沉淀的论点256解析:从题目中可以知道,碳元素,铝元素,镁元素比例为1:2:3,所以可以写成Mg3AlCO3,但是很快发现阴阳离子电荷数
我的理解
碳酸氢铵溶液基本上是接近中性或者更偏酸性一点
虽然氢氧化亚铁的离子积较低
但是碳酸根的浓度更大
所以会生成碳酸亚铁的沉淀
还有一个问题
氢氧化亚铁的溶度积=c(Fe2+)c(OH-)c(OH-)
碳酸亚铁的溶度积=c(Fe2+)c(CO32-)
无法得出氢氧化亚铁更容易沉淀的论点
25
6
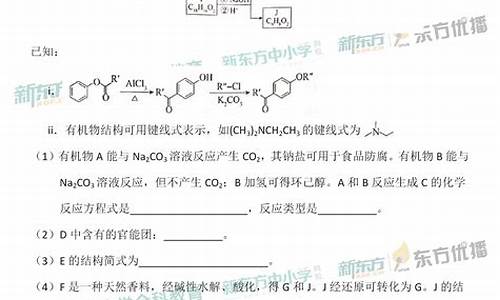
解析:从题目中可以知道,碳元素,铝元素,镁元素比例为1:2:3,所以可以写成Mg3AlCO3,但是很快发现阴阳离子电荷数不能抵消,所以需要引入氢氧跟,为了使物质呈电中性,需要引入2*3+3*2-2=10个氢氧跟,所以分子式为Mg3Al2(OH)10CO3
26
1
2,通空气,可以有效的减小氨气的浓度,是反应向生成氨气的方向进行。具体原理:空气在水中上升,空气本身不含氨气,水中的氨气会想气泡扩散,从而可以从水中带出部分氨气,还有,空气冲出水面,可以将水面上氨气浓度相对高的空气层吹散,降低的水面空气中氨气含量,有利于水中氨气逸出。
3
32克甲醇是1mol,转移了6mol电子,硝酸全部还原为氮气,每个硝酸可以提供5个电子(氮从正五价还原为零价),所以反应的硝酸的物质的量是6/5mol,硝酸是氧化剂,甲醇是还原剂,所以参加反应的还原剂和氧化剂摩尔比为1比6/5
即5:6